Почему радиус атома в периоде уменьшается
Глава 1.3.Структура периодической системы. Периодический закон. Д.И. Менделеева
Из более сотни известных химических элементов простые вещества неметаллы образуют 22 элемента, причем все они находятся в главных А подгруппах. Элементы-неметаллы находятся в правом верхнем углу Периодической таблицы, в главных подгруппах выше диагонали бериллий — астат. Причем с увеличением номера главной подгруппы число неметаллов в ней закономерно увеличивается на один рис.








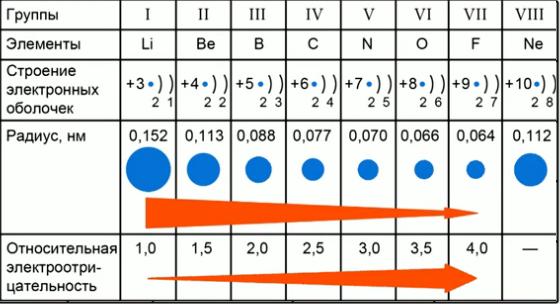

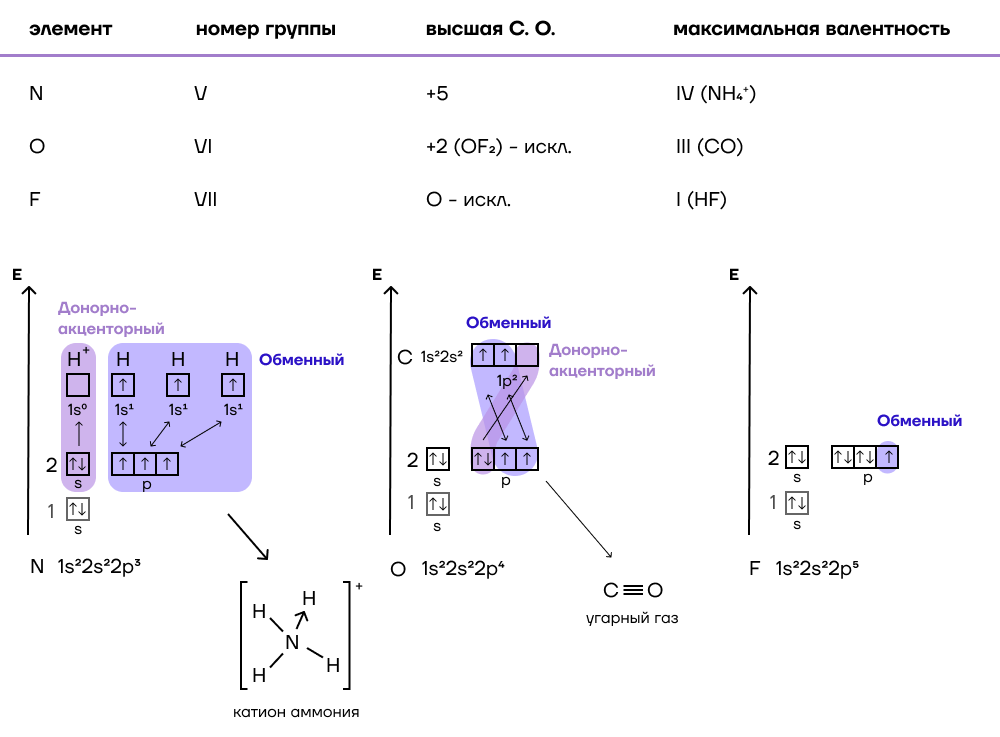
Подскажите, каким образом в периодической таблице Менделеева изменяется атомный радиус элементов? Действительно, в периоде атомный радиус уменьшается с увеличением порядкового номера элемента, то есть слева направо. Связано это с тем, что число электронных уровней атома не изменяется, но число электронов на внешнем уровне возрастает, а это приводит к усилению притяжения всей внешней оболочки атома к ядру. Соответственно и радиус атома уменьшается. В подгруппах же наблюдается обратная картина. Здесь с увеличением порядкового номера увеличивается число электронных орбит и заряд атома.
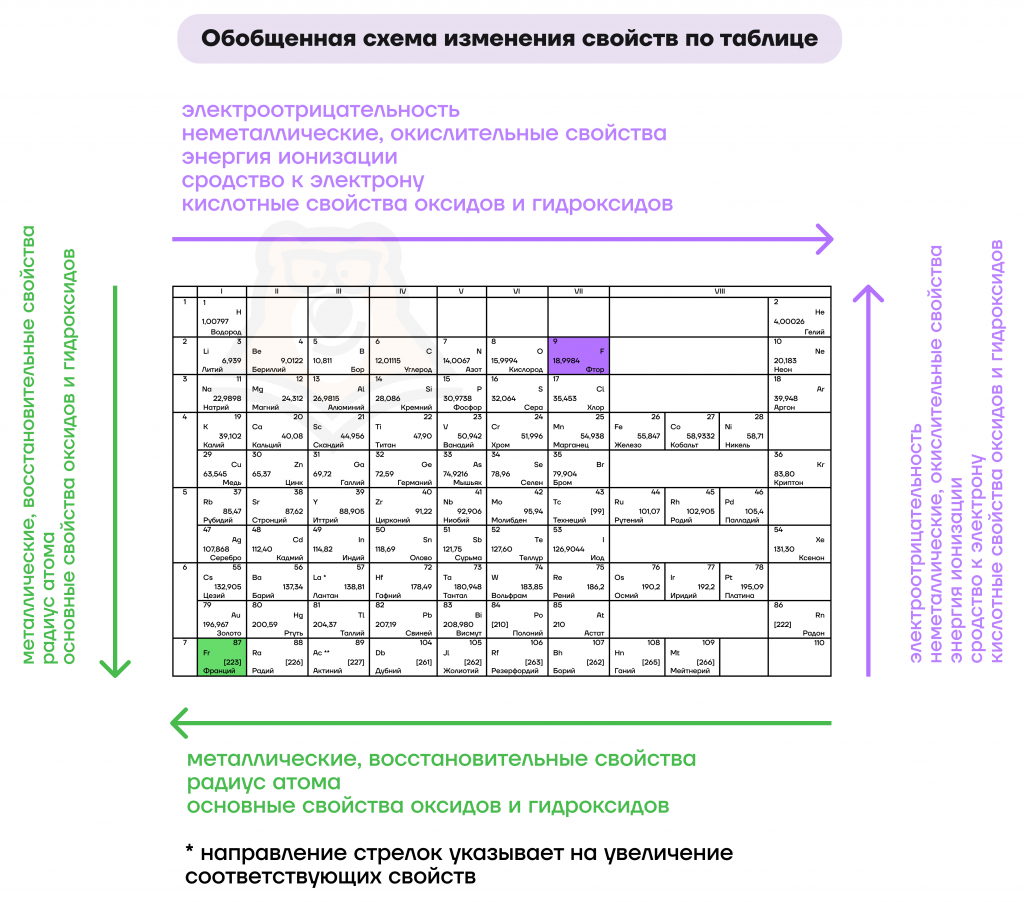
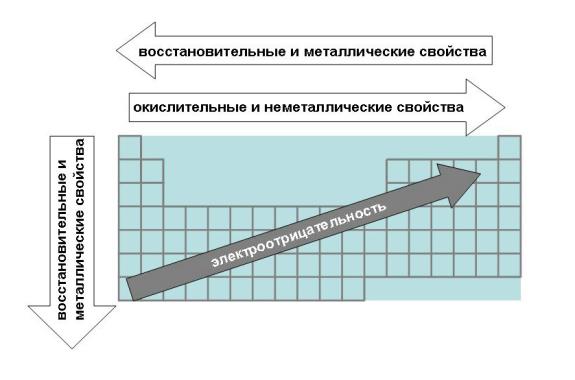


| 224 | Периодичность изменения радиусов атомов элементов. Радиус атома определяется размером его электронной оболочки. | |
| 260 | Все в мире подчиняется тем или иным законам: яблоко падает с дерева под силой тяжести, мы переходим дорогу только на зеленый свет, и в мире химии тоже есть свои законы. Химические элементы — «законопослушные граждане»! | |
| 442 | Вступите в симбиоз со Studarium и добавляйте сотни заданий в избранное :. | |
| 201 | Закономерности изменения свойств химических элементов и их соединений по группам и периодам Периодической системы Д. В соответствии с современными представлениями о строении атома, Периодический закон Д. | |
| 218 | Наименьший радиус атома из представленных элементов имеет. | |
| 232 | A subscription to JoVE is required to view this content. |
Поскольку атом не имеет определенных размеров, атомные радиусы представляют собой в известной мере условные величины. Различают орбитальные и эффективные атомные радиусы. Орбитальные радиусы r орб - это расстояния от ядра до главного максимума функции радиального распределения электронной плотности. Эти величины рассчитаны квантово-механическими методами для всех элементов периодической системы.